新聞網(wǎng)訊 非酒精性脂肪性肝?��。∟onalcoholic fatty liver disease, NAFLD)是最常見的慢性肝病之一�,已成為我國第一大肝病���,造成沉重的健康負擔���,非酒精性脂肪肝炎(nonalcoholic steatohepatitis,NASH)是NAFLD的惡性進展階段��,迄今為止尚未有藥物被批準用于治療NASH。環(huán)氧合酶(COX)是介導花生四烯酸代謝生成前列腺素和血栓烷的關(guān)鍵酶��,它包括COX1和COX2這兩種同工酶�����。通常認為在生理條件下�����,COX1是結(jié)構(gòu)酶�����,在很多組織中均有穩(wěn)定性表達�����,COX2是誘導酶���,只有在炎癥���、腫瘤等因素的刺激下可大量表達�����。COX2與炎癥�、腫瘤等關(guān)系的研究在過去三十年已取得了大量成果����,對COX1的關(guān)注則較少�,但近些年來研究發(fā)現(xiàn)COX1介導產(chǎn)生的功能遠比以前所認為的復雜�����。COX1在肝臟疾病中的機制研究很少被關(guān)注�����,在前期研究中���,香港大學團隊通過COX1全身敲除的小鼠模型�,發(fā)現(xiàn)COX1對化學肝損傷具有保護作用�����。
近日�����,青島大學附屬醫(yī)院任賀教授團隊聯(lián)合器官移植中心主任蔡金貞教授團隊/香港大學/暨南大學團隊在藥理學領(lǐng)域頂級期刊Acta Pharmaceutica Sinica B雜志(IF=14.9)在線發(fā)表了題為“Hepatic COX1 loss leads to impaired autophagic flux and exacerbates nonalcoholic steatohepatitis”的最新研究成果(https://www.sciencedirect.com/science/article/pii/S2211383523000977?via%3Dihub)��。
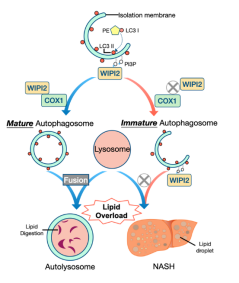
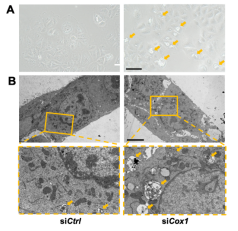
研究團隊首先通過臨床標本及多種小鼠模型肝臟樣本的檢測���,發(fā)現(xiàn)COX1在NASH中表達升高��,且與自噬水平呈相關(guān)����。為研究COX1在NASH進展中的潛在作用����,研究團隊通過建立三種不同的高脂飼料喂養(yǎng)飲食模型,發(fā)現(xiàn)肝細胞特異性敲除COX1可進一步加重自噬紊亂�����、肝臟脂質(zhì)堆積和炎癥反應病變��。通過進一步研究發(fā)現(xiàn)正常肝細胞中COX1可通過結(jié)合自噬小體形成的關(guān)鍵蛋白WIPI2形成成熟的自噬小體從而促進脂質(zhì)降解��,COX1缺失可能導致不成熟的自噬小體形成�����,在肝細胞脂肪堆積的病理狀態(tài)下��,從而加劇脂肪肝的進展��。在肝細胞COX1缺失的小鼠中采用腺相關(guān)病毒AAV-Wipi2回復WIPI2的表達可能通過促進成熟的自噬小體的形成從而延緩NASH進展�����,證實了COX1在NAFLD進展中具有重要的保護作用。上述研究首次提出了COX1可作為潛在的脂肪肝的治療靶點��,為臨床干預提供了新的理論依據(jù)�����。
青島大學附屬醫(yī)院于茜博士��、香港大學李暢博士和青島大學附屬醫(yī)院牛慶慧為該文共同第一作者�����,研究工作得到了國家杰出青年科學基金(82125026)���,國家優(yōu)秀青年科學基金(82122009)���,山東省自然科學基金(ZR2022QH241和ZR2020ZD11)的支持。






![]() 魯公網(wǎng)安備 37021202000856號
魯公網(wǎng)安備 37021202000856號 ![]()