新聞網訊 近日����,轉化醫(yī)學研究院于濤教授����、亓洪昭教授團隊在心血管靶向基因藥物遞送研究方面取得新進展���,研究發(fā)現了一個新的AAD治療靶點-tRF-Gly-CCC���,相關研究成果以“Activated neutrophil membrane-coated tRF-Gly-CCC nanoparticles for the treatment of aortic dissection/aneurysm”為題發(fā)表在《Journal of Controlled Release》(中科院期刊分區(qū)1區(qū),TOP期刊�����,IF=10.5)�。本文第一作者為轉化醫(yī)學研究院2021級碩士研究生李天翔和基礎醫(yī)學院楊艷艷副教授,通訊作者為于濤教授和亓洪昭教授����。該研究得到國家自然科學基金委、山東省自然科學基金委等項目資助�。
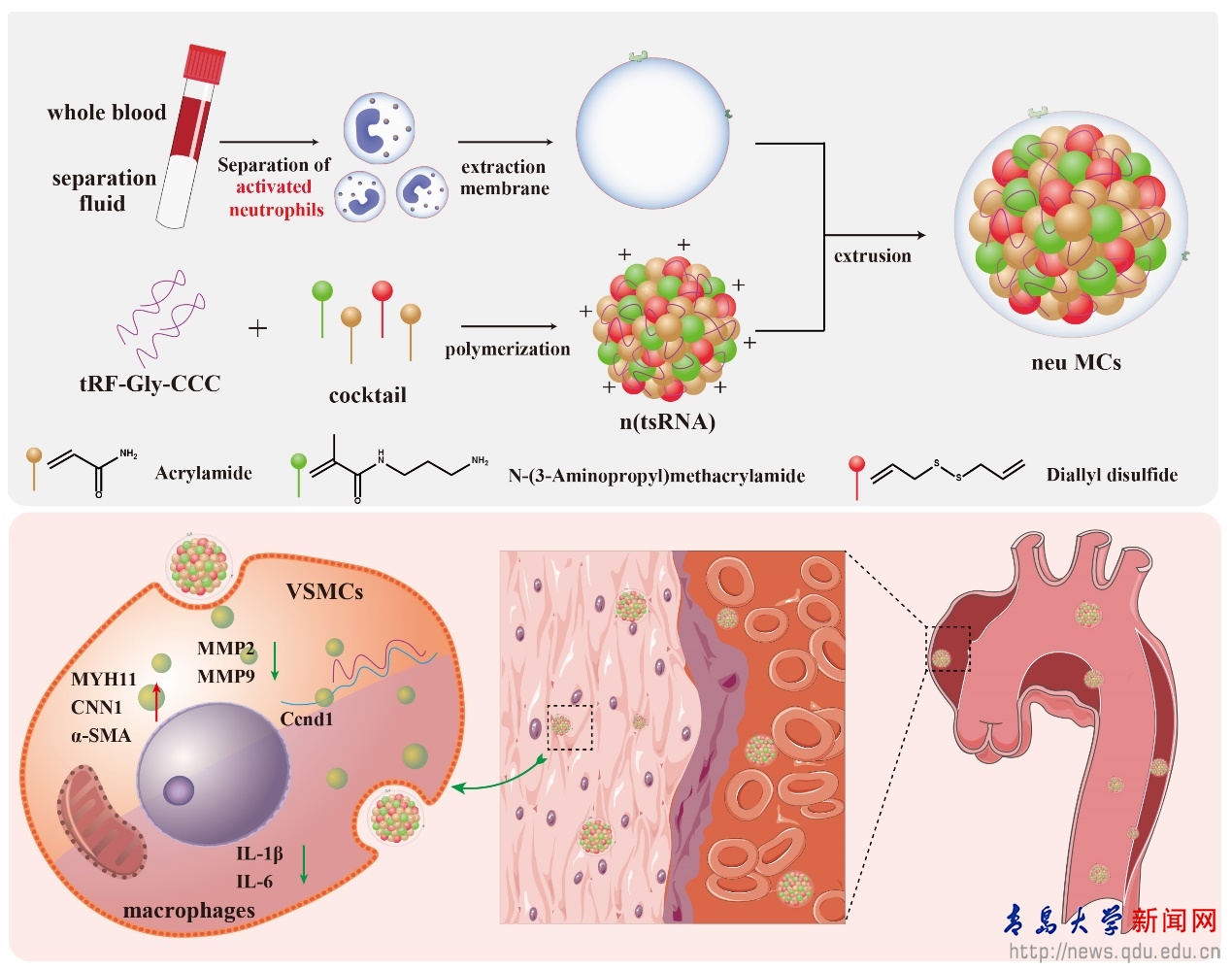
主動脈夾層/動脈瘤 (AAD) 是一種嚴重且危及生命的疾病,其特點是缺乏有效的主動防御藥物����,基因療法已成為治療AAD的一種有前景的方法。然而�,基因治療的臨床應用受到重大挑戰(zhàn)�,包括當前醫(yī)療實踐中創(chuàng)新基因藥物的稀缺以及缺乏簡化的基因藥物遞送體系�����。此研究聚焦在一個獨特的基因靶點 tRF-Gly-CCC 上���,它屬于一類小分子非編碼 tsRNA����,對維持血管平滑肌細胞功能和調節(jié)炎癥細胞反應至關重要�,但是在體內如何將基因藥物遞送到AAD病灶部位值得研究。因此���,于濤、亓洪昭團隊開發(fā)了一種基于活化的中性粒細胞膜為遞送體系的仿生納米顆粒 (neu MCs)���,以負載 tRF-Gly-CCC 的聚合物納米顆粒為核心藥物�����?���;罨闹行粤<毎ぞ哂须p重功能,即保護 tRF-Gly-CCC 的穩(wěn)定和促使核酸藥物靶向遞送至 AAD 位點�。在此基礎上,研究者構建的中性粒細胞膜仿生納米顆粒neu MCs實現了基因藥物的體內遞送����,有效緩解了AAD的發(fā)生率和死亡率,為下一步的核酸藥物臨床應用提供了新的防治方案��。






![]() 魯公網安備 37021202000856號
魯公網安備 37021202000856號 ![]()